Infection maternofœtale à parvovirus B19
Introduction
Le parvovirus B19 est un virus pathogène pour l'homme, responsable d'infections généralement bénignes : le mégalérythème épidémique, maladie infantile courante (ou 5ème maladie) et des arthropathies plus fréquemment constatées chez l'adulte. Sa pathogénicité est plus importante chez les patients immunodéprimés et en cas d'infection maternofœtale. Lors d'une infection chez la femme enceinte, le passage du virus de la mère à l'enfant à travers le placenta peut entraîner des atteintes fœtales, débutant par une anémie et aboutissant dans certains cas à la mort intra-utérine du fœtus. Une exposition au virus en cours de grossesse nécessite donc une surveillance particulière pour détecter précocement la contamination chez la mère et une éventuelle infection chez le fœtus.
I. Rappel virologique
La famille des Parvoviridae rassemble des virus non enveloppés d'environ 20 nm de diamètre, à capside icosaédrique contenant une molécule génomique d'ADN monocaténaire d'environ 5500 nucléotides. Le genre Parvovirus regroupe les parvovirus autonomes possédant toute l'information génétique nécessaire à leur réplication et qui infectent de nombreux vertébrés.
Le parvovirus B19 est un virus strictement humain et il appartient au genre Erythrovirus, compte tenu de son tropisme cellulaire très restreint avec une réplication sélective dans les précurseurs de la lignée érythrocytaire ; découvert fortuitement en 1975 dans des sérums de donneurs de sang asymptomatiques et dénommé HPV (human parvovirus), il est appelé actuellement virus B19 (initiale identifiant la poche de sang où il fut trouvé la première fois).
II. Epidémiologie des infections à parvovirus B19
La transmission du virus se fait principalement par la voie respiratoire : il se propage par les sécrétions respiratoires ou par des contacts des mains sur la bouche. C'est un virus ubiquitaire qui sévit sur le mode endémo-épidémique ; il est à l'origine de petites épidémies de fin d'hiver et de début de printemps chez des sujets contacts non immuns, avec parfois une notion familiale. La séroprévalence augmente avec l'âge : elle est de 2 à 10% avant 5 ans, et de 40 à 60% chez les adultes de 20 à 60 ans. L'infection survient donc le plus souvent chez les jeunes enfants, mais peut s'observer chez l'adulte jeune.
Le passage transplacentaire du virus de la mère au fœtus se produit dans 1/3 des cas de primo-infection chez une femme enceinte. Environ 50% des femmes en âge de procréer ne sont pas immunisées et l'exposition au virus, lors d'une grossesse, comporte un risque de transmission maternofœtale. Les femmes courant le plus de risques sont les mères d'enfants d'âge préscolaire et scolaire, les puéricultrices et les institutrices, ainsi que le personnel soignant pédiatrique.
Le virus peut être transmis par transfusion sanguine lorsque le don de sang provient d'un sujet en phase virémique et encore asymptomatique ; en effet le virus B19, thermostable, dépourvu d'enveloppe, est très résistant, et n'est pas inactivé par les procédés physico-chimiques utilisés pour éliminer les virus enveloppés (VIH, HBV, HCV) dans les produits sanguins. Ce mode de transmission est cependant exceptionnel.
III. Physiopathologie de la primo-infection et manifestations cliniques chez l'enfant et l'adulte
La pénétration du virus dans l'organisme par voie respiratoire est suivie, environ une semaine après la contamination, d'une phase de virémie, au cours de laquelle le virus atteint ses cellules cibles. Le récepteur cellulaire du parvovirus B19 est l'antigène P érythrocytaire situé principalement sur les précurseurs des érythroblastes ; le virus bloque la maturation des proérythroblastes entraînant une érythroblastopénie se traduisant par une diminution du nombre des réticulocytes pendant plusieurs jours. A la fin de cette 1ère phase, apparaissent des anticorps neutralisants IgM puis IgG anti-parvovirus B19 qui éliminent rapidement le virus.
La virémie se manifeste par un syndrome pseudo-grippal avec une sensation de malaise, des céphalées, une fébricule, des courbatures, et parfois une rhinopharyngite. Environ 2 à 3 semaines après le contage, chez certains sujets, apparaissent un rash cutané ou des douleurs articulaires.
Les manifestations cliniques dépendent d'un équilibre entre la réplication virale et la réponse immunitaire de l'hôte. Elles sont différentes selon le statut immunologique et hématologique du sujet infecté.
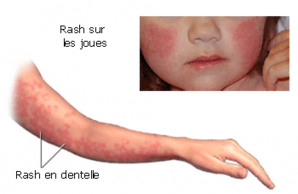 | 20 à 25% des adultes infectés par le parvovirus B19 sont asymptomatiques. Les principales manifestations cliniques sont l'érythème et les arthralgies. |
La primo-infection se traduit par l'apparition d'un érythème maculopapuleux, débutant au niveau des joues et donnant un aspect souffleté au visage, puis s'étendant au tronc et aux extrémités sous la forme de macules roses pâles. Cette maladie éruptive bénigne, appelée aussi la 5ème maladie, concerne surtout les enfants avant 10 ans lors de petites épidémies en milieu scolaire. L'incubation peut durer jusqu'à 3 semaines, et la contagiosité est maximale dans la période précédant les signes cliniques. Les symptômes disparaissent spontanément après 5 à 10 jours.
Les manifestations articulaires sont présentes seulement dans 10% des cas d'infection chez l'enfant. Elles sont plus fréquentes chez l'adulte et en particulier chez la femme. Elles consistent en l'apparition de polyarthrites bilatérales et symétriques, d'installation brutale, affectant les mains, les poignets, les genoux et les chevilles, douloureuses mais peu sévères ; dans 90% des cas l'amélioration se fait en 2 à 3 semaines et il n'y a pas de séquelles articulaires.
Comme pour l'érythème infectieux aigu, l'apparition de l'arthrite coïncide avec la mise en place de la réponse immune et l'augmentation des anticorps IgM puis IgG ; les manifestations cliniques sont essentiellement liées à la formation de complexes immuns. La réticulopénie liée à la diminution transitoire des érythroblastes n'a pas de conséquence clinique ; les hématies du sujet sain ayant une durée de vie normale de 120 jours, il n'y a pas d'anémie chez le sujet normal.
Chez les patients atteints d'anomalies hématologiques sous-jacentes fragilisant les globules rouges (drépanocytose, thalassémie, sphérocytose, déficit en G6PD, en pyruvate kinase etc...) et déjà porteurs d'une anémie hémolytique, l'infection se manifeste sous la forme de crise érythroblastopénique entraînant une anémie transitoire brutale.
De rares cas d'infections chroniques liées à l'immunodépression, quelle qu'en soit la cause, se manifestent par une érythroblastopénie profonde et durable, sans qu'il y ait de pathologie hémolytique sous-jacente. La réponse immune humorale, insuffisante, est incapable de maîtriser la multiplication virale. Ceci explique également l'absence des autres symptômes, rash cutané et/ou arthralgies.
Le parvovirus B19 a été occasionnellement mis en en cause dans des cas de myocardite, de neuropathie, de purpura thrombopénique, de purpura vasculaire, de syndrome appendiculaire, de neutropénie auto-immune, de détresse respiratoire.
Des thrombopénies, ainsi que des neutropénies, peuvent accompagner, voire révéler, une infection par le virus B19.
IV. Infection maternofœtale
En France, environ 50% des femmes en âge de procréer sont immunisées et ont des anticorps anti parvovirus B19 protecteurs. Seule la primo-infection chez les femmes enceintes séro-négatives peut avoir des conséquences sur le fœtus.
La fréquence du passage transplacentaire du virus a été évaluée à 33%. Une femme enceinte, dont le statut sérologique n'est pas connu et qui a été en contact avec le virus, risque d'être contaminée dans 10% des cas, et la probabilité que le fœtus soit infecté est alors d'environ 3%.
On manque de données précises en France sur l'impact de l'infection fœtale.
Elle peut être suspectée en cas de signes cliniques évocateurs, devant une éruption ou l'apparition de douleurs articulaires au cours de la grossesse, mais elle est le plus souvent asymptomatique.
C'est surtout la notion de contage chez une femme enceinte récemment exposée au virus, soit professionnellement, soit au contact de ses propres enfants, en période d'épidémie, qui doit faire penser à une éventuelle primo-infection de la mère ; il faut alors vérifier rapidement le statut immunitaire de la mère, même en l'absence de symptômes, pour détecter la présence d'anticorps spécifiques anti-parvovirus B19 et une séroconversion.
Dans la majorité des cas, la primo-infection maternelle est sans conséquence fœtale.
Dans environ 10% des cas, les risques principaux sont les avortements spontanés, la mort fœtale in utero et l'anasarque fœto-placentaire.
C'est au cours de la virémie chez la femme enceinte contaminée que le passage transplacentaire du virus peut avoir lieu et entraîner une atteinte du fœtus, car le virus est lytique pour les précurseurs érythroïdes fœtaux ; le fœtus est particulièrement sensible au virus car son hématopoïèse est très active et sa réponse immunitaire immature. Les hématies fœtales ayant une durée de vie plus courte, l'infection entraîne une anémie plus ou moins grave responsable d'une hypoxémie et d'une hyperviscosité sanguine ; une insuffisance cardiaque et des anomalies fonctionnelles hépatiques provoquent des œdèmes sous-cutanés et des épanchements chez le fœtus, ainsi qu'un œdème du placenta. Cet œdème généralisé caractérise l'anasarque fœtoplacentaire qui survient en général durant le 2ème trimestre de la grossesse et plus rarement au cours du 3ème trimestre.
Selon les études, le risque de mort fœtale intra-utérine, lors d'une infection aiguë chez la mère, varie de 5 à 9% ; le décès du fœtus est souvent lié à une anasarque.
Il a été également constaté que le taux d'avortements spontanés est plus élevé lorsque l'infection est contractée avant 20 semaines de gestation que lorsqu'elle l'est après 20 semaines.
-
Tests sérologiques en cours de grossesse
Le diagnostic de l'infection à parvovirus B19 chez la femme enceinte doit être précoce et repose sur la sérologie spécifique par la mise en évidence des anticorps IgM ou d'une séroconversion IgG grâce à des tests immunoenzymatiques suffisamment sensibles.
Les IgM apparaissent de 10 à 15 jours après le contage et peuvent subsister pendant 6 mois. Les IgG apparaissent quelques jours après les IgM et persistent généralement toute la vie.
-
La présence isolée des IgG spécifiques après une exposition récente témoigne en principe d'une infection ancienne et indique l'immunité.
-
La présence des IgM en l'absence d'IgG témoigne d'une primo-infection récente. (Attention, il peut s'agir de faux positifs et il est nécessaire de contrôler les IgM).
-
Si les tests sont négatifs, la femme n'est pas immunisée et reste vulnérable à l'infection ; mais si elle a été récemment exposée au virus et si l'infection est en phase d'incubation, il faut refaire les tests 2 à 4 semaines plus tard.
-
La présence simultanée d'IgG et d'IgM peut aussi être le signe d'une infection récente, à condition de révéler, à 15 jours d'intervalle, une augmentation des anticorps IgG par l'analyse d'un 2ème sérum (séroconversion).
Mise en évidence d'une infection à Parvovirus chez la femme enceinte
-
Diagnostic des infections fœtales
Si une femme fait réellement une primo-infection (prouvée sérologiquement), le virus peut être transmis au fœtus et il faut organiser un suivi spécialisé par un gynécologue-obstétricien.
- Surveillance échographique hebdomadaire pendant 8 à 12 semaines.
- L'apparition d'œdèmes fœtoplacentaires doit faire suspecter une infection du fœtus par le parvovirus B19 et une anasarque.
- Mise en évidence de l'ADN viral par PCR dans le liquide amniotique ou dans le sang de cordon : méthode de diagnostic virologique direct de référence, réalisée uniquement si une atteinte fœtale est révélée par l'échographie.
En cas de survenue d'une anasarque fœtoplacentaire, la ponction du sang fœtal permet aussi de doser l'hémoglobine et, si l'anémie fœtale est sévère (hémoglobine inférieure à 80g/L), de réaliser dans le même temps une transfusion sanguine in utero.
La guérison est obtenue par ce traitement dans 75% des cas.
Seulement 20% des cas d'anasarque guérissent spontanément ; dans 80% des cas, en l'absence de traitement, elle entraîne la mort fœtale.
Il n'existe pas actuellement de traitement antiviral efficace de l'infection maternelle et fœtale.
Devant la rareté des complications fœtales après primo-infection maternelle, un dépistage systématique des infections à parvovirus B19 chez la femme enceinte par un suivi sérologique n'est pas justifié.
Références
-
Parvoviridae. F.Morinet, C.Pallier, S.Pillet
Traité de Virologie Médicale. 2003 ; chap. 20, pages 283-289. Ed. Estem
-
Le parvovirus B19. F. Morinet.
Virologie Médicale. A. Mamette. 2002 ; chap.34, pages 453-457
-
Infection maternofœtale à parvovirus B19. M.H. Poissonnier, P. Lebon
Infections virales et toxoplasmose maternofœtales. 2001 ; pages 47-57. Ed.Elsevier
-
Infections au parvovirus B19 en cours de grossesse.
Directives cliniques de la Société des Obstétriciens et Gynécologues du Canada.septembre 2002
-
Information et recommandations du Ministère de la Santé sur le site Internet : http://www.sante.gouv.fr/htm/dossiers/parvovirus/sommaire.htm
Infections à Parvovirus B19-point d'actualité - juillet 2005
