Méloxicam : rôle du groupe méthylthiazole
Le groupement 5-méthylthiazole du MÉLOXICAM module à la fois la sélectivité d'action et le profil toxicologique de la molécule.
![]() MÉCANISME DE L'INHIBITION PRÉFÉRENTIELLE DE LA COX-2
MÉCANISME DE L'INHIBITION PRÉFÉRENTIELLE DE LA COX-2
Les interactions entre le MÉLOXICAM et le site actif de la COX-2 ont fait l'objet d'une étude récente (XU, 2014). Elles sont schématiquement représentées dans la figure suivante :
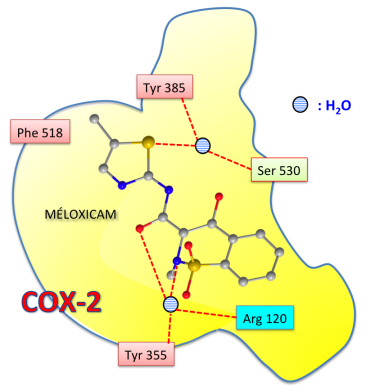
Le mécanisme de fixation fait intervenir un réseau de liaisons hydrogène impliquant essentiellement les résidus Arg 120, Tyr 355, Ser 530 et Tyr 385. Les interactions ligand-enzyme sont indirectes et se font par l'intermédiaire de deux molécules d'eau interposées.
![]() MODULATION DES TRANSFORMATIONS MÉTABOLIQUES
MODULATION DES TRANSFORMATIONS MÉTABOLIQUES
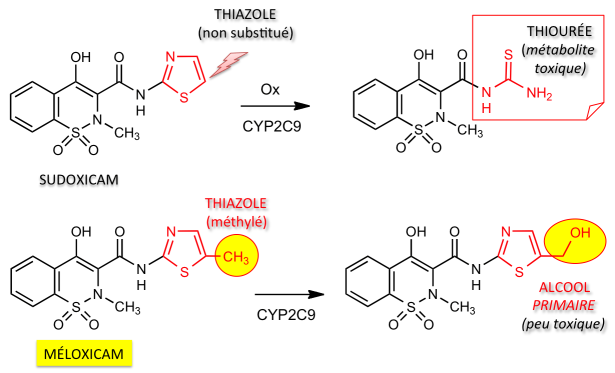
Le substituant CH3 en position 5 sur le cycle thiazole joue un rôle fondamental dans la protection de la molécule vis-à-vis de la métabolisation par les cytochromes P450. Cette propriété a été mise en évidence sur le dérivé thiazolique non substitué (SUDOXICAM) : en l'absence de groupe CH3, le métabolisme oxydatif conduit à l'ouverture du cycle thiazole, avec formation d'une thio-urée hépatotoxique
![]() Cet effet indésirable a été à l'origine du retrait du SUDOXICAM.
Cet effet indésirable a été à l'origine du retrait du SUDOXICAM.
Dans le MÉLOXICAM, le cycle thiazole protégé par le CH3 ne peut pas subir de dégradation métabolique directe : l'action du cytochrome conduit à l'oxydation du méthyle en fonction alcool primaire (métabolite peu toxique, facilement éliminé, après oxydation en acide).