Solubilité
Les complexes de platine antitumoraux se distinguent par leur hydrosolubilité variable d'un dérivé à l'autre. Paradoxalement, ce sont les complexes organiques qui présentent la meilleure hydrosolubilité comparativement au cisplatine.
CISPLATINE | CARBOPLATINE | OXALIPLATINE | |
|---|---|---|---|
EAU (25 °C) | ≈ 2 mg/mL | ≈ 16 mg/mL | ≈ 8 mg/mL |
Alcool, acétone | — | < 0,4 mg/mL | — |
![]() CISPLATINE
CISPLATINE
Sa très faible solubilité dans l'eau (voisine de 1 mg/mL) constitue un problème pour la préparation des solutés injectables.
![]() CARBOPLATINE
CARBOPLATINE
Le carboplatine est pratiquement dix fois plus hydrosoluble que le cisplatine : cette surprenante propriété est attribuée aux ligands CARBOXYLATO dont les atomes d'oxygène, riches en doublets libres, fonctionnent comme des accepteurs de liaisons hydrogène.
L'hypothèse de l'établissement de liaisons hydrogène entre le carboplatine et les molécules d'eau environnantes est étayée par deux observations :
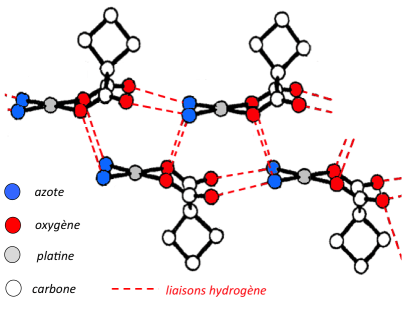
Les travaux de NEIDLE sur le carboplatine à l'état cristallin, ont mis en évidence de nombreuses liaisons H intermoléculaires. Ces liaisons H se forment entre complexes inclus dans la maille cristalline et font intervenir :
d'une part, les atomes d'oxygène des ligands carboxylato ;
d'autre part, les hydrogènes des ligands ammine appartenant à un complexe adjacent.
D'autres travaux (DI PASQUA, 2011) sur des solutions aqueuses concentrées de carboplatine ont montré que des liaisons H du même type semblent également exister et sont à l'origine de la formation de dimères. Ces auto-associations pourraient expliquer, en partie, la grande stabilité du carboplatine en solution aqueuse.
![]() OXALIPLATINE
OXALIPLATINE
Le motif cyclohexane, par son caractère hydrophobe, est un facteur limitant à l'égard de l'hydrosolubilité (la solubilité de l'oxaliplatine est environ deux fois plus faible que celle du carboplatine)
