Extinction de fluorescence
-
Les processus de extinction de fluorescence, encore appelée inhibition de fluorescence ou quenching sont des processus bimoléculaires et leur efficacité dépend fortement de la distance entre les réactifs.
-
Pour la description de la dynamique de quenching, il est important de distinguer les cas où la diffusion est possible et ceux où elle ne l'est pas.
-
D'une manière générale l'extinction de fluorescence peut être du à 2 types d'interaction.
-
Quenching "statique" : complexe préformé à l'état fondamental
-
Quenching "dynamique" : extinction dépendant de la diffusion
-
-
Cest un quenching sans diffusion.
-
La distance entre le donneur et le quencher est fixe.
-
Il y a formation d'un complexe non fluorescent à l'état fondamental.
-
-
Ce processus se manifeste lorsque l'inhibiteur est localisé au voisinage immédiat du chromophore excité.
-
Cette interaction, quasi instantanée, est trop rapide pour être décelée expérimentalement sur la courbe de déclin de fluorescence de sorte que la durée de vie moyenne mesurée est celle du chromophore non soumis à ce type d'interaction.
-
La diminution de fluorescence correspond à une diminution de la concentration en molécules fluorescentes.
-
-
Un tel processus provoque donc une réduction du rendement quantique sans affecter la durée de vie moyenne et entraîne ainsi une diminution du rapport

-
Ce processus dépend de la concentration on sera donc gêné si forte concentration en inhibiteur
-
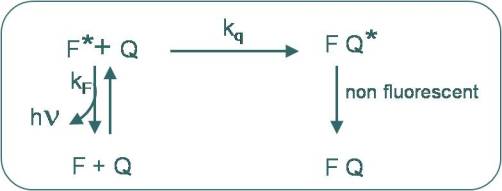
C'est un quenching avec diffusion : le quenching dynamique résulte d'une interaction bimoléculaire contrôlée par la diffusion entre un chromophore excité et un inhibiteur
-
Dans ce cas, le quenching a lieu chaque fois qu'une molécule de quencheur diffuse dans la zone de réaction.
-
Le quenching dynamique est caractérisé par un rapport
 constant
.
constant
.
 cste_inhibition[Zoom...] | I0 = intensité de fluorescence en absence d'inhibiteur t0 = durée de vie moyenne en absence d'inhibiteur I = intensité de fluorescence en présence d'inhibiteur kq = constante cinétique de la réaction KSV = constante de Stern-Volmer |
-
Différents inhibiteurs : O2, halogènes (iode brome, fluor) , acrylamide
-
L'effet dépend de la molécule inhibitrice et de l'affinité (un même inhibiteur n'a pas le même effet sur les chromophores).
