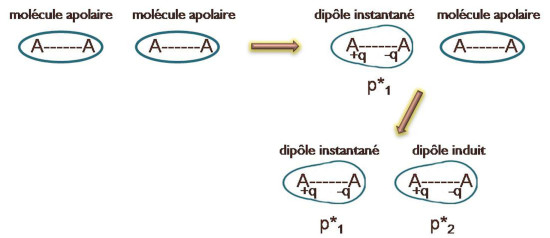
Forces de dispersion de London
Ces interactions se produisent entre 2 molécules apolaires.
-
interaction dipôle induit-dipôle induit
Dans de telles molécules, les électrons qui constituent le nuage électronique sont perpétuellement en mouvement sur leur orbite.
Ces fluctuations spatiales font que la molécule à chaque instant peut présenter un dipôle électrique instantané (bien que, en moyenne, le moment dipolaire soit nul).
Il existera donc des interactions électrostatiques instantanées qui vont donner une cohésion aux liquides ou au solides.
| 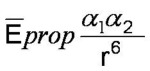 energie_london |
-
La probabilité de création de dipôle instantané est lié à la propriété de la molécule, à ses oscillations et donc à sa déformation .