Pression osmotique
-
L'existence du flux indique que le système n'est pas en équilibre
-
On pourrait rétablir cet équilibre en exerçant sur la solution une pression hydrostatique suffisante pour annuler le flux de solvant .
-
Afin d'empêcher une telle migration on doit fournir une pression supplémentaire , appelée pression osmotique, égale à la valeur de la pression hydrostatique s'opposant au phénomène . (En d'autres termes la pression osmotique est la pression hydrostatique qu'il faudrait exercer sur la solution pour empêcher le solvant pur de traverser la membrane qui sépare les 2 phases).
L'osmose fut découverte par Dutrochet (1826) qui imagina un appareil (osmomètre) constitué d'un réservoir de verre rempli d'une solution sucrée colorée ( sorte de cylindre vertical dont la base est obturée par une membrane hémiperméable (vessie de porc) et dont la partie supérieure est reliée à un long tube vertical de petit calibre) et plongé dans un cristallisoir contenant de l'eau.
| 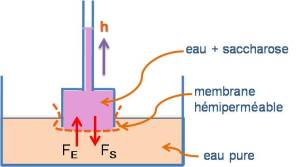 osmometre[Zoom...] |
Cette ressource peut être visualisée en plein écran, pour cela cliquer sur le bouton en bas à droite dans la barre de défilement. Cliquer ensuite pour faire apparaître les différents éléments de la vidéo. La touche Echap permet de quitter le diaporama.
La pression osmotique est, par définition, la pression qu'il faudrait exercer sur une solution pour l'amener à un état d'équilibre (=absence de flux net) avec le solvant dont elle est séparée par une membrane à perméabilité sélective.
-
Deux solutions dont les pressions osmotiques sont égales sont dites " isotoniques "
-
En cas d'inégalité, elles sont " hypertoniques " ou " hypotoniques " l'une par rapport à l'autre, une solution étant choisie comme référence .
-
La solution la plus concentrée en soluté est dite hypertonique par rapport à l'autre.
-
La solution la moins concentrée en soluté (solution diluée) est dite hypotonique par rapport à l'autre.
-
Dans l'organisme, les secteurs cellulaires, interstitiels, intravasculaires sont autant de compartiments séparés par des membranes à perméabilité sélective, généralement différente d'un type à l'autre. Des phénomènes osmotiques vont intervenir entre ces différents compartiments.
