Mesure de M
L'osmose est la première méthode de mesure de la masse moléculaire des protéines.
-
L'influence de la pression étant facilement mesurable, l'une des applications les plus courantes de l'osmométrie est la mesure des masses molaires des macromolécules (protéines et polymères synthétiques). Ces molécules énormes donnant des solutions loin d'être idéales, on suppose que l'équation de van'tHoff est seulement le 1er terme de développement d'une équation du viriel :
-
Dans le cas de solutions macromoléculaires, les résultats dépendent de la concentration de la solution. Donc on ne peut pas faire une mesure directe de M par une seule mesure de .
-
En effet, si on porte en fonction de C, on devrait obtenir une droite horizontale. Or ceci est très rarement observé. On obtient expérimentalement des droites plus ou moins inclinées.
-
On remarque d'autre part que si on recommence l'expérience dans d'autres solvants, on obtient d'autres droites mais ces droites passent toutes par la même origine.
-
Donc pour déterminer la masse molaire, il suffit d'extrapoler à C nulle.
-
On porte $\frac{\pi}{C$ en fonction de C
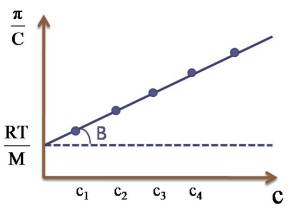 mesure_M[Zoom...] | On obtient une droite. L'ordonné à l'origine permet de calculer M
Le coefficient directeur B est une constante empirique, dite coefficient osmotique du viriel. Ce coefficient dépend du couple solvant/soluté . NB : Cette technique convient bien pour des valeurs de M élevées (M>30000Da). Pour de petites valeurs de M, les pressions sont énormes et il est difficile de fabriquer des membranes hémiperméables. |
Ces droites apportent 2 informations :
-
B > 0 signifie que l'attraction du solvant sur les macromolécules est très forte (molécule déployée) le solvant attire fortement la macromolécule, le solvant déplie la macromolécule.
-
B ≈ 0 le solvant a peu d'interaction sur la macromolécule et la macromolécule est repliée sur elle-même.
-
B < 0 (rare) la macromolécule est peu soluble dans le solvant – solution instable.
On obtient ainsi des informations sur la masse et sur les interactions soluté-solvant donc indirectement sur la forme de la macromolécule.
