Acides et dérivés – R de Claisen – R de Dieckmann
Question
Dans le cours, on n’a pas de détails sur la réaction de Claisen. Est-ce que vous pourriez donner le mécanisme complet ?
Appelée aussi condensation de Claisen, la réaction de Claisen est une réaction de préparation des β cétoesters par condensation de deux esters en milieu alcalin. Le mécanisme est le suivant :
-
Avec une base forte (alcoolate), arrachage d'un hydrogène en α de la fonction ester.
-
Addition du carbanion obtenu (nucléophile) sur une deuxième mole d'ester et formation d'un intermédiaire tétraédrique (flèches vertes sur le mécanisme).
-
Elimination d'un alcoolate sur l'intermédiaire tétraédrique et formation du β cétoester (flèches roses).
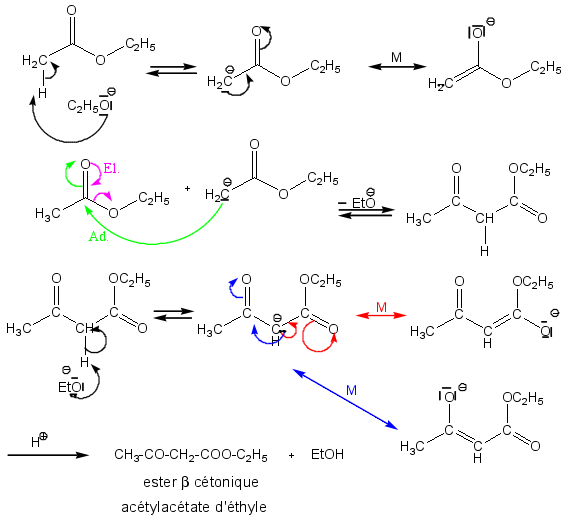
En fait le β-cétoester est formé à la fin de la deuxième ligne du mécanisme ci-dessus. Cependant, ce produit est acide (les hydrogènes du groupement CH2 en α de l'ester et de la cétone sont très acides - bases conjuguées très stables) et l'éthylate formé au cours de la réaction arrache un hydrogène; on obtient un sel qu'il suffit de placer en milieu acide pour obtenir définitivement l'ester β-cétonique.
Si les deux fonctions esters sont portées par le même composé, il se forme également un ester β-cétonique par cyclisation intramoléculaire. C’est la réaction de Dieckmann et son mécanisme est identique à celui de Claisen.
