Alcènes – Elimination d'Hofmann
Question
Je n’ai pas compris pourquoi avec l’élimination d’Hofmann on ne forme pas l’alcène le plus substitué.
Quand on élimine un sel d’ammonium en milieu basique (E2), on obtient effectivement l’alcène le moins substitué. C’est l’élimination d’Hofmann et cette réaction est anti-Zaïtsev.
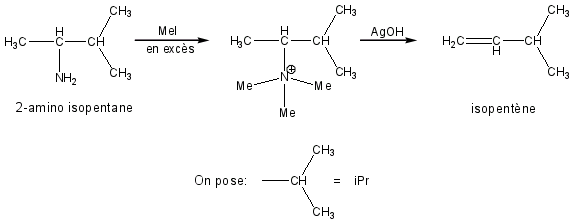
Soit le 2-amino isopentane. Traité par de l'iodure de méthyle en excès on obtient le sel d'ammonium correspondant. L'élimination de ce sel en milieu alcalin (AgOH) conduit majoritairement à l'isopentène.
Comme il y a un atome d'hydrogène de chaque côté du groupement ammonium, deux éliminations sont possibles. Cette élimination est d’ordre 2, donc stéréospécifique (trans).
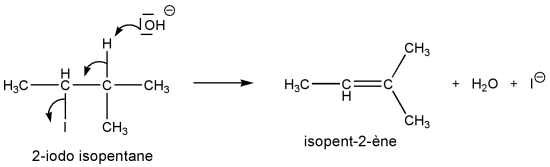
Dans l'élimination supposée E2 d'un hydracide sur un halogénoalcane, l'halogénure est un bon groupe partant (surtout l'iodure) et l'arrachage de l'atome d'hydrogène par la base et le départ de X sont synchronisés. L'état de transition de cette réaction présente déjà l'ébauche de la future double liaison, et il est d'autant plus stable que la double liaison à venir est plus substituée (règle de Zaïtsev)
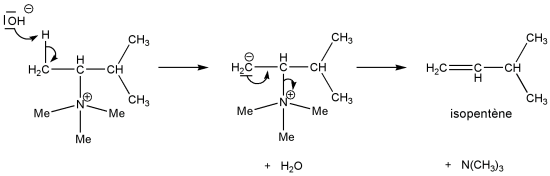
Dans l'élimination d'un sel d'ammonium selon Hofmann, l'amine est un mauvais groupe partant (nucléofuge) et le mécanisme est différent du précédent. L'arrachage de l'atome d'hydrogène précède le départ de l'amine. Il en résulte l'apparition d'une charge négative sur l'état de transition : l'état intermédiaire est anionique, et c'est bien sûr l'anion le plus stable qui va se former c'est à dire celui qui est le moins substitué par des groupements donneurs inductifs (C1). Il est à remarquer que les atomes d'hydrogène des carbones les moins substitués sont également les plus acides.
L’élimination du sel d’ammonium sur le 2-triméthylammonium isopentane donne majoritairement l’isopentène. L’isopent-2-ène est le produit minoritaire.
Le produit majoritaire est l’alcène le moins substitué. L’élimination du sel d’ammonium selon Hofmann ne suit donc pas la règle de Zaïtsev.